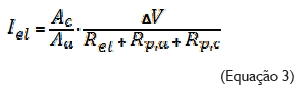Artigos
Parafusos estruturais de aço patinável na construção em aço - Parte Final
Premiado oito vezes e dono de um curriculo exuberante, o doutor Fábio D. Pannoni conclui seu artigo sobre aços patináveis
Área do cátodo e anodo.jpg)
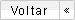
Este é um ponto crítico quando se pensa em parafusos e consumíveis de soldagem, em geral. Um importante fator no cálculo da densidade da corrente da cela galvânica, Iel (corrente de cela relacionada à área) é a razão das áreas superficiais catódica (Ac) e anódica (Aa). Ela influencia tremendamente a velocidade da corrosão galvânica (Equação 3):
Sempre que a área superficial do catodo (o componente mais nobre do par galvânico) for muito menor do que a área superficial do anodo (a liga metálica menos nobre), nenhuma mudança no comportamento frente à corrosão é costumeiramente observada. Esta situação é ilustrada na Figura 6.
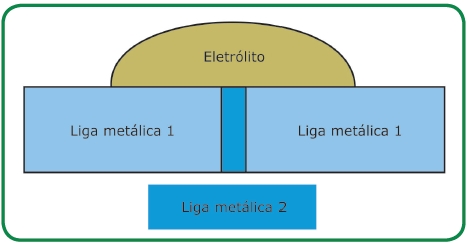
Figura 6: Enquanto a área superficial do catodo (Liga metálica 2) for pequena comparada à do anodo (Liga metálica 1), nenhum dano é observado ao anodo (Liga metálica 1).
Exemplos típicos podem ser encontrados quando parafusos de aço patinável são utilizados em componentes de aço carbono. Não há corrosão dos componentes de aço carbono e a ligação é preservada. A Figura 7 ilustra uma situação ainda mais extrema – a união de aço carbono galvanizado a quente com aço inoxidável, sem problemas de origem galvânica. Mesmo em ambientes relativamente agressivos (classificação C4, segundo a ISO 9223), não há corrosão galvânica!
Sob condições atmosféricas, torna-se, por vezes, difícil quantificar as proporções ativas das superfícies anódicas e catódicas de uma estrutura. Para uma avaliação prática, entretanto, isto é desnecessário. Normalmente, basta considerar o sistema em geral. Na combinação de materiais, parafusos devem ser sempre feitos de materiais mais nobres, de modo que a superfície catódica seja pequena. Este conceito está descrito em muitos livros que tratam do tema corrosão – e possui forte embasamento teórico. Assim, o uso de parafusos (e consumíveis de solda) com características “patináveis”, em estruturas de aço patinável ou não, garante a integridade estrutural do conjunto ao longo do tempo.
A situação oposta, entretanto, pode causar problemas. Se um anodo pequeno for conectado a um grande catodo (por exemplo, um parafuso de aço carbono – galvanizado ou não – conectado a componentes estruturais de aço patinável), a corrosão galvânica poderá ocorrer (Figura 8).

Figura 7: Parafusos de aço inoxidável conectados em componentes de aço carbono de área superficial muito maior não promovem a corrosão galvânica. Em ambos os casos, as conexões estão em ambiente externo, classificado segundo a norma ISO 9223 como C3 (ambiente de alta agressividade).
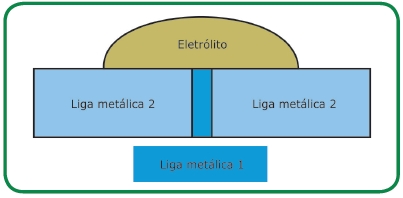
Figura 8: A corrosão galvânica pode ocorrer se a área superfi cial do anodo (Liga metálica 1) for pequena, e, a do catodo, grande. Este é o caso da utilização de parafusos estruturais “pretos” ou galvanizados a quente em estruturas de aço patinável.
Experiência prática
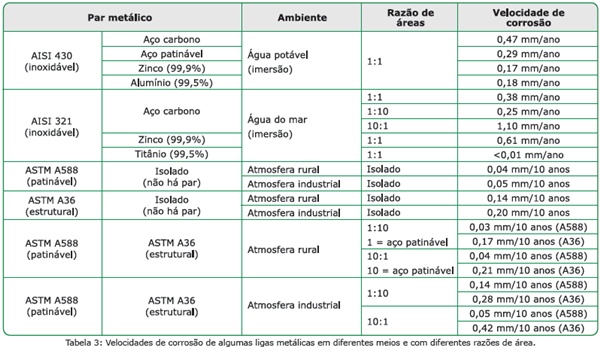
Existe uma grande quantidade de informação na literatura a respeito da combinação dos aços carbono com diferentes ligas metálicas, em diferentes ambientes. A Tabela 3 traz algumas destas informações disponíveis na literatura.
A corrosão galvânica de componentes expostos à atmosfera somente pode ocorrer durante os períodos de exposição à umidade. A superfície não precisa entrar em contato diretamente com, p.ex., chuva. A deposição de sujeira e fuligem tem influência significativa sobre os períodos de umidade, pois, através de vários mecanismos, mantém a superfície umedecida permanentemente.
Frestas pouco aeradas podem levar à presença constante de umidade. Em contraste com os elementos imersos em sistemas aquosos, o desenvolvimento da corrosão galvânica atmosférica somente ocorre em uma área bastante limitada, próxima do ponto de união das duas ligas metálicas. A corrosão ocorre, neste caso, somente em uma pequena região, ao longo da linha de contato, sem que a maior parte da superfície metálica restante desempenhe qualquer papel efetivo.
Conclusões
1. A corrosão galvânica é um fenômeno eletroquímico que somente se manifesta quando duas ou mais ligas metálicas, que apresentam diferentes potenciais eletroquímicos, conectadas “eletricamente”, são banhadas por um mesmo eletrólito;
2. As conhecidas “Tabela de Potenciais de Eletrodo Padrão” ou as “Tabelas de Série Galvânica” não são, por si só, indicadores da possível ocorrência da corrosão galvânica;
3. Os fatores mais importantes para o desenvolvimento da corrosão galvânica são, por ordem de importância:
a. Área relativa dos componentes anódicos e catódicos. Sempre que a área do anodo for muito maior (> 10x) que a do catodo, nenhuma corrosão galvânica ocorrerá em ambientes classificados pela norma ISO 9223 como de muito baixa agressividade (C1), baixa agressividade (C2, média agressividade (C3) e alta agressividade (C4). O inverso é potencialmente perigoso: grandes áreas catódicas (> 10x) conectadas a pequenas áreas anódicas poderão levar ao desenvolvimento da corrosão galvânica, para as mesmas condições ambientais descritas;
b. Resistividade do eletrólito. O risco da corrosão galvânica diminui grandemente com o aumento da resistividade do eletrólito. Eletrólitos gerados em ambientes rurais (classificação C2) e urbanos (classificação C3 e C4), não favorecem o aparecimento da corrosão galvânica. Em contrapartida, os ambientes industriais e marinhos (C5-I e C5-M, respectivamente) merecem atenção.
4. Parafusos estruturais de aço patinável (ASTM A325 Tipo 3) podem - e devem ser - os escolhidos nas ligações de estruturas confeccionadas em aço estrutural ao carbono ou aço patinável. Isso se deve ao fato de que, quando aplicados em estruturas constituídas em aços estruturais, garantem a integridade da ligação ao longo dos anos. A corrosão não ocorre devido à razão de áreas anódica/catódica favorável. O mesmo pode ser dito para as estruturas constituídas em aços patináveis.
5. Parafusos estruturais de aço carbono (ASTM A325 Tipo 1), em contrapartida, não devem ser utilizados em estruturas de aço patinável, sob risco do aparecimento da corrosão galvânica. A razão de áreas (anódica/catódica) não favorece esta aplicação. O mesmo pode ser dito com respeito ao uso destes mesmos parafusos, galvanizados a quente.
Referências
1. X. G. Zhang, “Galvanic Corrosion”. In: Uhlig´s Corrosion Handbook, 3rd. edition, Editor R. Winston Revie, John Wiley, Hoboken, N.J., 2011.
2. H. Kaesche, “Metallic Corrosion – Principles of Physical Chemistry and Current Problems”, Tradução de R. A. Rapp, National Association of Corrosion Engineers – International (NACE), 1985.
3. V. Kucera e E. Mattson, “Atmospheric Corrosion of Bimetallic Structures”. In: Atmospheric Corrosion, Editor W.H. Ailor, John Wiley, New York, 1982.
4. H.E. Townsend, C.D. Gorman e R.J. Fischer, Atmospheric corrosion performance of hot-dip galvanized bolts for fastening weathering steel guiderail, Corrosion 98, NACE International, paper no. 344.
5. K.P. Fischer, A review of offshore experiences with bolts and fasteners, Corrosion 2003, NACE International, paper no. 3017.
Fabio Domingos Pannoni
Bacharel em Química pelo Instituto de Química da USP, Mestre e Doutor em Engenharia Metalúrgica pela Escola Politécnica da Universidade de São Paulo. Consultor Técnico da Gerdau Aços Brasil e do CBCA – Centro Brasileiro da Construção em Aço. Professor do Programa de Educação Continuada em Engenharia (PECE) da Escola Politécnica da USP. Possui duas patentes de aços e mais de sessenta artigos técnicos publicados no Brasil e no exterior. Autor e co-autor de quatro livros publicados. Recebeu oito prêmios de reconhecimento, dentre os quais se destacam o “Prêmio Jovem Cientista” (CNPq, Grupo Gerdau e Fundação Roberto Marinho), “Prêmio Governador do Estado” (Governo do Estado de São Paulo) e “Prêmio Talento Brasileiro” (FIESP). fabio.pannoni@gerdau.com.br |
 Edições on-line
Edições on-line  Fale Conosco
Fale Conosco 


 CONTEÚDO DA EDIÇÃO
CONTEÚDO DA EDIÇÃO




 Edição 103
Edição 103.jpg)